放射医学与辐射防护国家重点实验室、放射医学与防护学院史海斌教授课题组在化学干预细胞核内DNA抗肿瘤耐药方面取得新进展,相关成果以“Self-Generative Singlet Oxygen (1O2)-Initiated Chemical Modification of Nuclear DNAs Combats Tumor Drug Resistance”为题于6月3日在线发表在国际知名期刊Journal of the American Chemical Society上。论文链接:https://doi.org/10.1021/jacs.5c02826。
近年来,尽管化疗在临床肿瘤治疗中发挥着关键的作用,但多药耐药(MDR)问题已成为影响临床肿瘤治疗疗效的主要障碍。研究表明,MDR的产生涉及细胞内药物浓度下降、靶点结构改变、代谢解毒增强、DNA损伤修复失衡等多个方面。针对这一难题,开发精准高效的治疗策略以逆转或克服耐药机制,已成为当前肿瘤治疗研究的热点方向,具有重要的科研意义和临床价值。
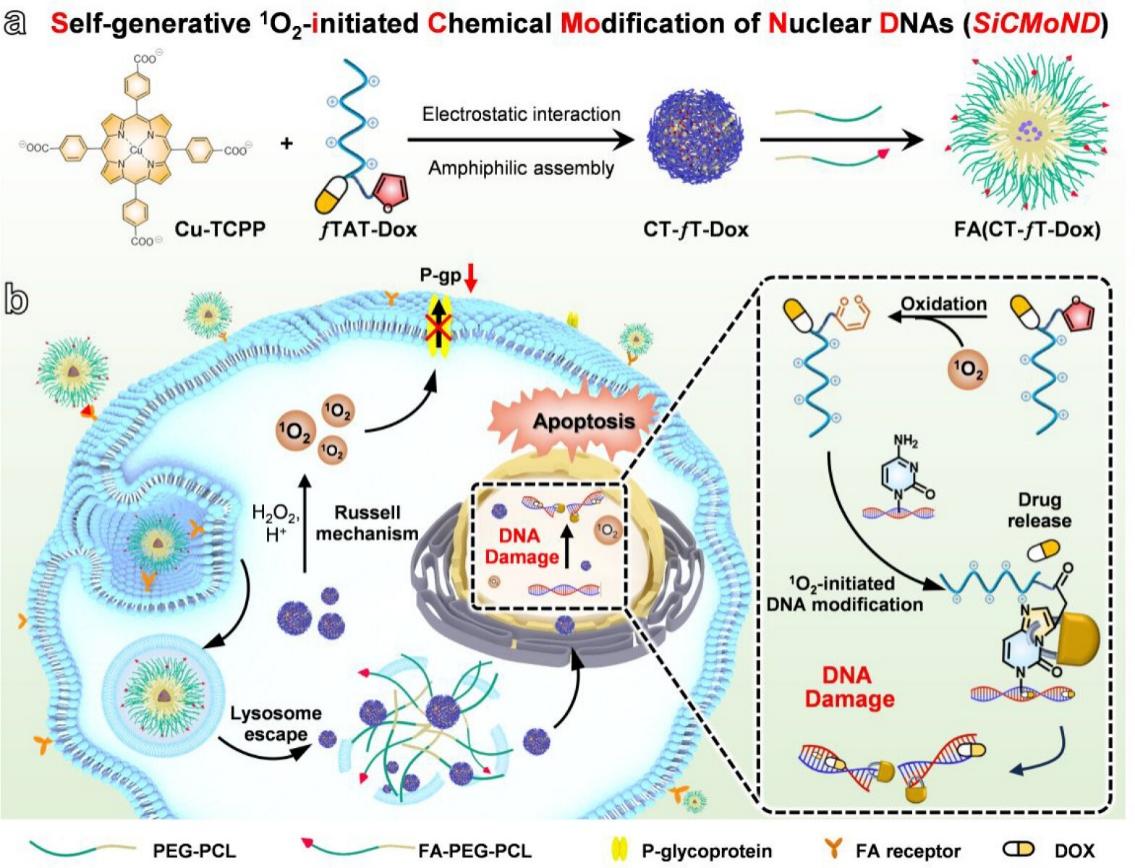
在前期研究中,史海斌教授课题组已经开发了一系列先进的RNA共价化学修饰抗肿瘤治疗新策略,实现了对细胞质RNA(J. Am. Chem. Soc.2020, 142, 21502;J. Am. Chem. Soc.2022, 144, 23061)和线粒体RNA(Angew. Chem. Int. Ed. 2023, 62, e202218969)的精准高效抑制和功能干预,为恶性肿瘤的精准治疗提供了全新思路。在最新研究中,史海斌教授课题组创新性发展了一种由自生单线态氧(1O2)引发的细胞核DNA化学修饰新策略SiCMoND。该策略可协同传统化学治疗,一定程度上克服肿瘤的耐药,达到优异的抗肿瘤治疗效果。该系统通过将在肿瘤微环境中自发产生1O2的Cu-TCPP和修饰有呋喃基团和阳离子跨膜肽的前药¦TAT-Dox共同包载于叶酸修饰的PEG-PCL胶束中,成功制备得到一种肿瘤靶向的“纳米炸弹”FA(CT-¦T-Dox)。该纳米药物可被肿瘤细胞特异性摄取,在肿瘤微环境中释放Cu-TCPP和¦TAT-Dox。首先,Cu-TCPP在瘤内高浓度的H2O2产生大量1O2,从而触发前药中的呋喃与细胞核DNA的碱基发生共价环化反应,实现对肿瘤细胞核DNA的化学修饰及功能干预,有效延长DOX药物在核内的滞留时间,同时协同核内DNA的损伤效应,实现MDR肿瘤的高效治疗。该SiCMoND策略在耐药乳腺癌模型中表现出优异的治疗效果,为突破肿瘤多药耐药难题提供了新思路和新方法。
苏州大学苏州医学院放射医学与防护学院2020级博士研究生王安娜为该论文第一作者,国重室史海斌教授为通讯作者。该研究得到了国家自然科学基金项目、江苏省基础研究计划项目、苏州市基础研究计划项目、放射医学与辐射防护国家重点实验室开放课题等资助。
(撰稿人王安娜,第一审稿人史海斌,审稿人王成奎,第一校稿人王安娜,第二校稿人史海斌,校稿人徐加英)