放射医学与辐射防护国家重点实验室、放射医学与防护学院史海斌教授课题组在纳米疫苗原位制备增强肿瘤放射免疫治疗方面取得新进展,相关成果以“Light-mediated In-situ Synchronous Capture of Antigens and Nucleic Acids as Nanovaccines to Boost Tumor Radioimmunotherapy”为题于4月7日在线发表在国际知名期刊Journal of the American Chemical Society上。论文链接:https://pubs.acs.org/articlesonrequest/AOR-DNM8RV2P6VMHBYIMEWZP。
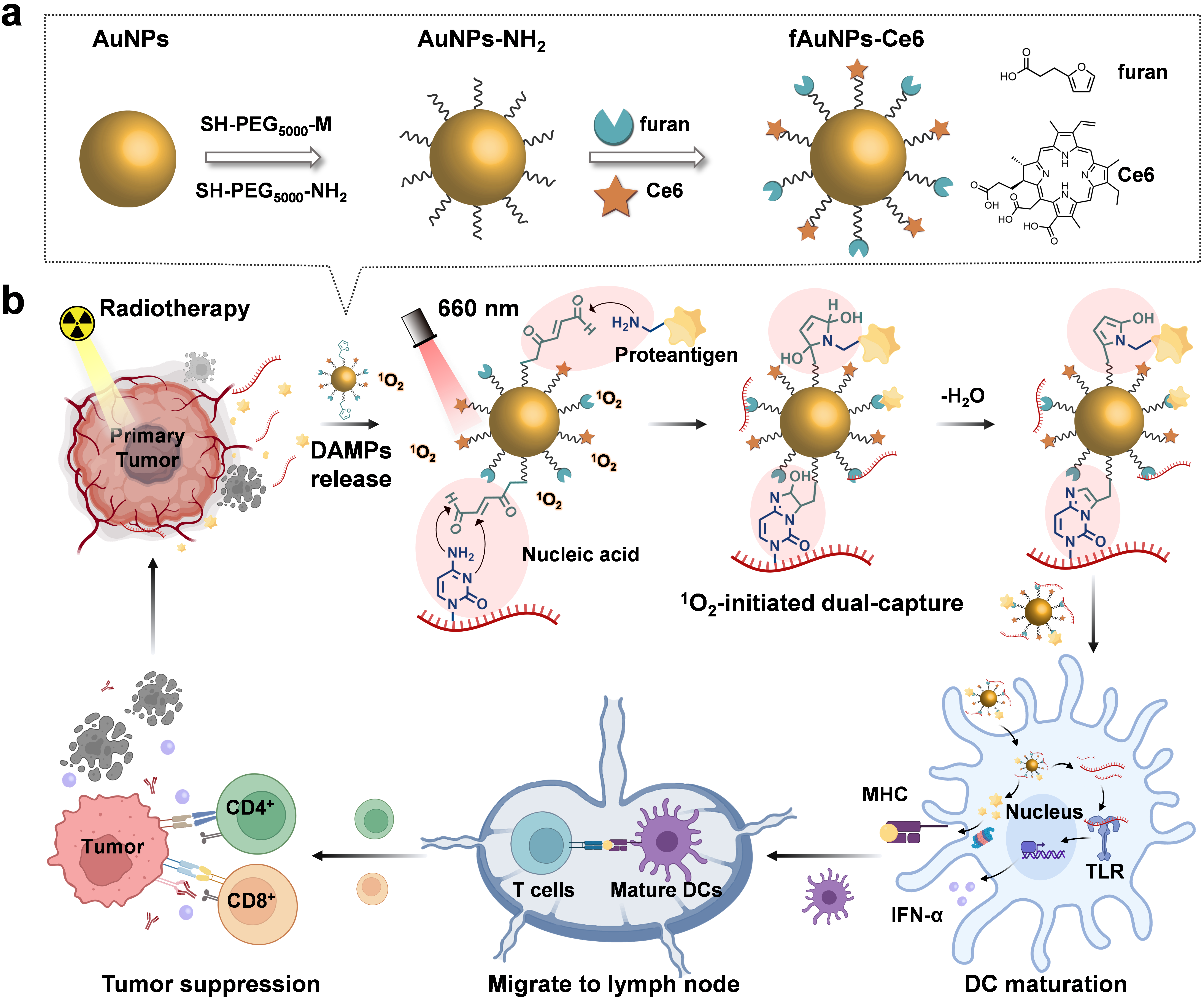
图1.红光介导的瘤内同步共价捕获抗原蛋白与核酸分子制备纳米疫苗用于增强肿瘤放射免疫治疗研究的示意图
癌症疫苗作为一种新型的免疫治疗手段在肿瘤治疗中展现出巨大潜力,目前主要包括肿瘤抗原疫苗、mRNA疫苗及树突状细胞(DCs)疫苗等。然而,这些疫苗大多依赖体外制备,靶向抗原种类有限且新抗原预测复杂,严重制约了其临床应用范围。相比之下,原位疫苗接种(ISV)具有抗原谱广、个体化适配性强等优点,近年来备受关注。放疗是诱导ISV的重要方式之一,可通过引起肿瘤细胞免疫原性死亡,释放大量肿瘤相关抗原、肿瘤特异性抗原以及损伤相关分子模式,从而激活机体抗肿瘤免疫反应,产生远隔效应。然而,大量研究发现肿瘤抗原和损伤相关分子模式易被内源性蛋白酶或核酸酶降解清除,导致DCs摄取不足,严重限制了该策略的临床转化。因此,开发精准高效的抗原捕获新策略对于提升ISV的免疫效应至关重要
在前期研究中,史海斌教授课题组已经开发了一系列先进的核酸共价化学修饰抗肿瘤治疗新策略,实现了对细胞质RNA(J. Am. Chem. Soc.2020, 142, 21502;J. Am. Chem. Soc.2022, 144, 23061)、线粒体RNA(Angew. Chem. Int. Ed.2023, 62, e202218969)以及细胞核DNA(J. Am. Chem. Soc.2025, 147, 20534-20547)的精准高效化学修饰与功能干预,为恶性肿瘤的精准高效治疗提供了全新思路。在最新研究中,我们创新性设计并构建了一种呋喃和Ce6修饰的金纳米颗粒fAuNPs-Ce6。在660 nm激光的照射下,光敏剂Ce6产生大量单线态氧(1O2)催化呋喃通过共价反应同步捕获肿瘤抗原蛋白质和核酸片段。该策略不仅大幅延长抗原和佐剂在肿瘤微环境的保留时间,还在不依赖外源佐剂的条件下高效促进树突状细胞成熟,进而引发强大的全身抗肿瘤免疫反应。尤为值得关注的是,将这种原位纳米疫苗与PD-L1阻断疗法联用,可显著提升放射治疗效果,有效抑制原发和远处肿瘤的生长。该光调控的原位疫苗接种新策略,为恶性肿瘤的精准治疗提供了一种富有前景的新思路。
苏州大学苏州医学院放射医学与防护学院2025级博士研究生李苗为该论文第一作者,国重室史海斌教授为通讯作者。该研究得到了国家自然科学基金项目、江苏省基础研究计划项目、苏州市基础研究计划项目、放射医学与辐射防护国家重点实验室开放课题等资助。
撰稿人李苗、第一校稿人程侠菊、第二校稿人史海斌、第三校稿人徐加英、第一审稿人史海斌、第二审稿人徐加英、第三审稿人王成奎